Nuestro equipo de enfermería es el primero en entrar en contacto con el paciente, por lo tanto, será de suma importancia que sepa reconocer el aspecto y las medidas a tomar ante la sospecha del biofilms.
Índice
Definición:
El biofilm es una estructura compleja y dinámica formada por microorganismos vivos que forman una comunidad, protegida por una membrana, sobre una superficie biótica o abiótica. Es una comunidad heterogénea formada, a menudo, por diferentes bacterias y hongos y dinámica, dado que estos se reproducen y pueden migrar. Las agrupaciones de estos microorganismos se envuelven en una membrana, formada por exopolisacáridos que emiten las propias células de cuerpo y agua que en su conjunto constituyen una estructura, dentro de la cual alojarse y permanecer protegidos. Aunque la matriz de los exopolisacáridos es lo suficientemente sólida como para proteger a la comunidad microbiana de los agentes antimicrobianos, los antibióticos o el sistema inmunológico del paciente; sí permiten el paso del oxígeno, agua y nutrientes para seguir creciendo. Tan compleja es la estructura del biofilm, que los microorganismos que lo constituyen son capaces de generar una señal de comunicación entre ellos, para atraer más comunidades y organizarse.
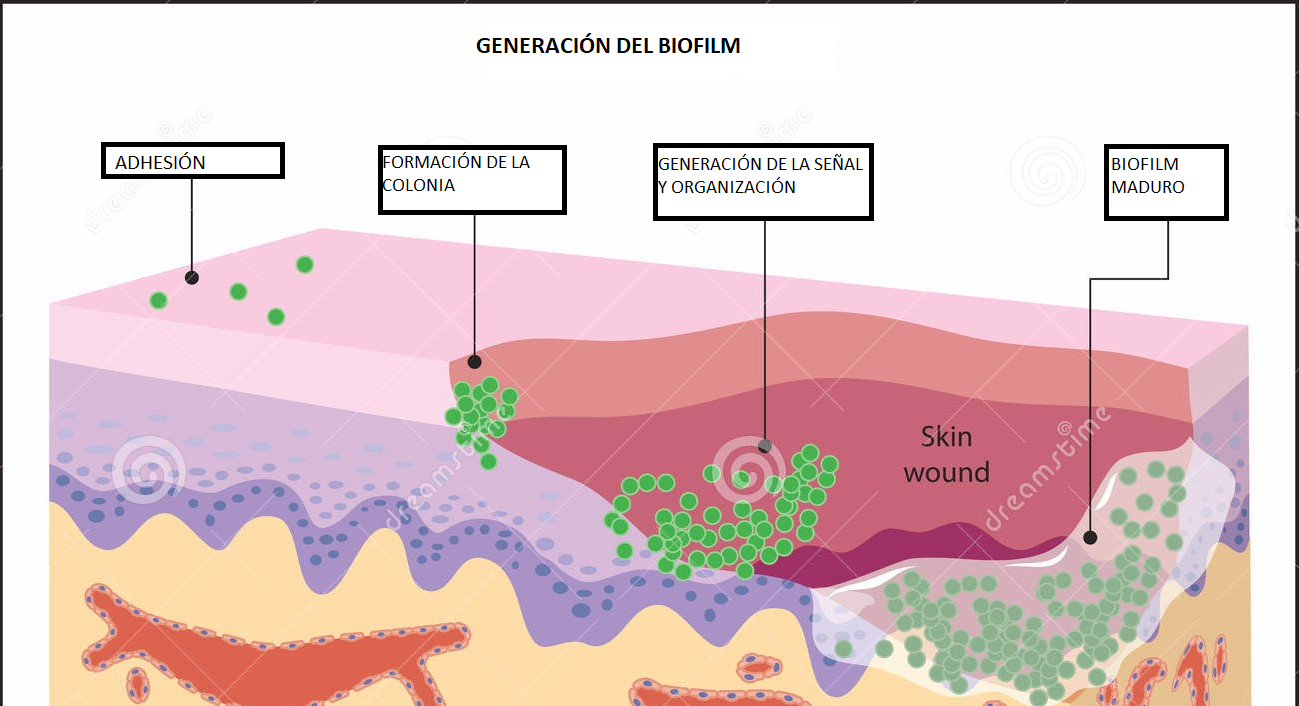
Cómo es el proceso de formación de un biofilm
- Adhesión reversible a la superficie, la fase inicial, llevada a cabo por un microorganismo solitario (estado planctónico).
- Una actuación correcta en esta fase por parte del equipo de curas evitará la creación del biofilm.
- Adhesión irreversible a la superficie: la fase en la cual los microorganismos comienzan a multiplicarse y a organizarse para procurar la supervivencia de la comunidad formada. Biofilm/ matriz protectora y su diseminación a otras zonas.
El biofilm y las heridas
Los biofilms suelen estar presentes en las heridas crónicas, y se cree que contribuyen a un estado inflamatorio crónico que retrasan o impiden la cicatrización. Por lo tanto, el mejor indicador clínico de sospecha sobre su presencia será el retraso en el proceso de cicatrización.
Existen evidencias de que el 60%- 100% de las heridas crónicas presentan biofilm, al menos en alguna zona del lecho, en comparación con el solo 6% en las agudas.
Para detectar la existencia del Biofilm en una úlcera se precisa de la toma de muestra de tejido/exudado, que se puede realizar mediante diferentes técnicas, la más utilizada es “el método Levine”. Este método consiste en frotar con un hisopo el lecho de la herida, desbridada y desinfectada previamente, recogiendo muestra del mayor exudado posible, normalmente se tendrá que realizar sobre la zona que está en peor condición clínica, evitando los bordes. Otro método, quizá el más recomendado, sería la biopsia del tejido de la herida, proporciona unos resultados más fiables, pero es menos utilizado que el anterior. Una vez obtenidas las muestras para el cultivo, en el laboratorio se realizará un estudio específico de éstas.
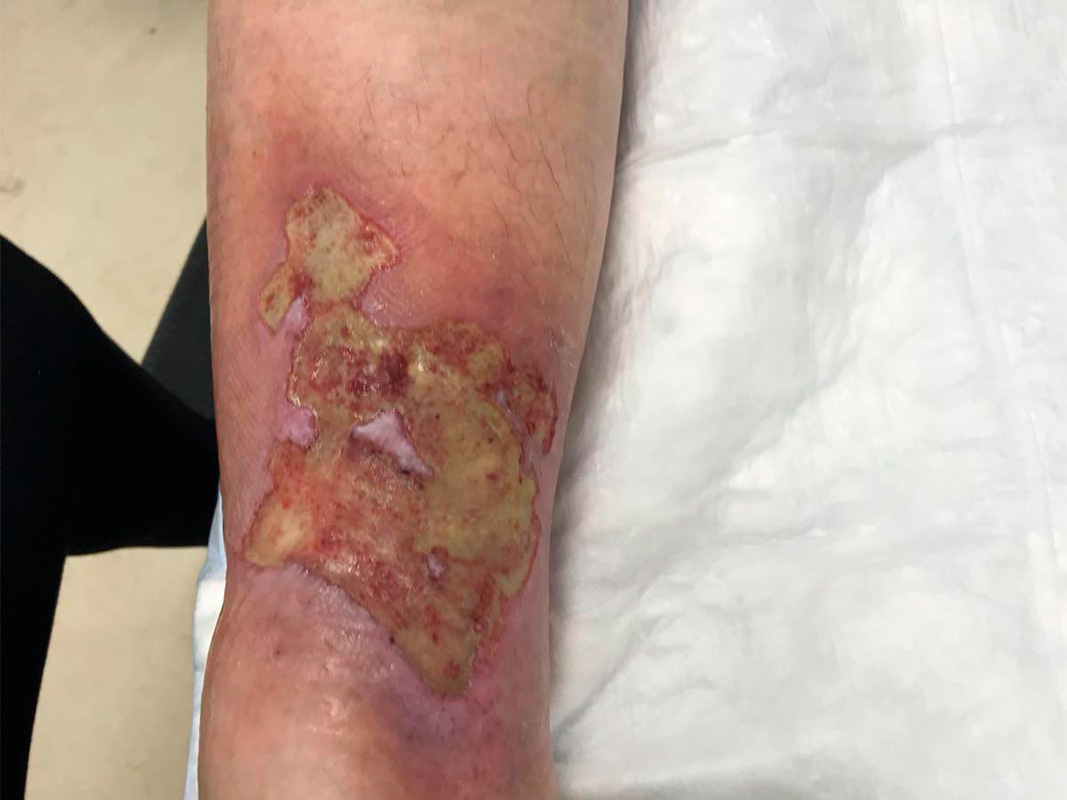
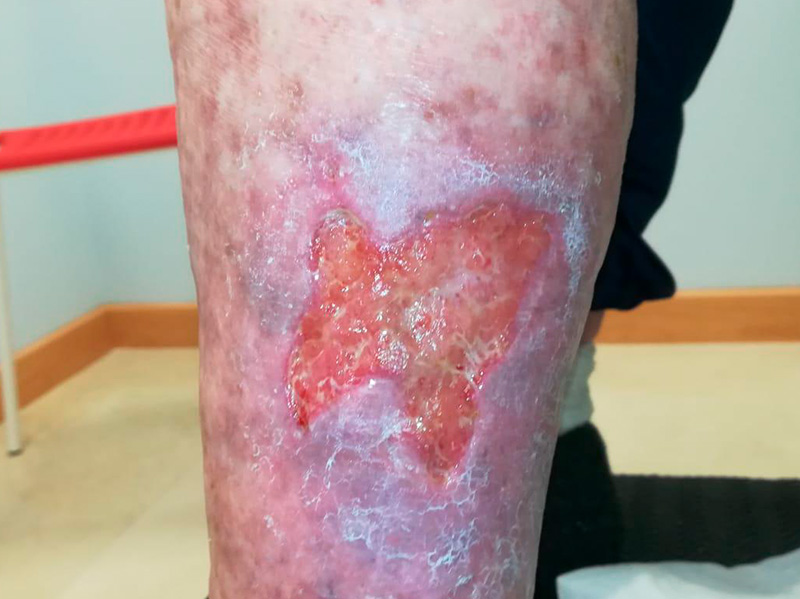
- ¿Se puede observar el biofilm a simple vista?
La respuesta es algo ambigua, existen signos que nos pueden sugerir la presencia de biofilm en una herida, pero siempre tendrán que apoyarse en un cultivo. Estos serían, a parte de los signos y síntomas de una infección, presencia de fibrina desnaturalizada y esfacelo cubiertos por una película brillante, pobre respuesta a los tratamientos tópicos y sistémicos, aumento del dolor y aumento del tamaño de la herida.
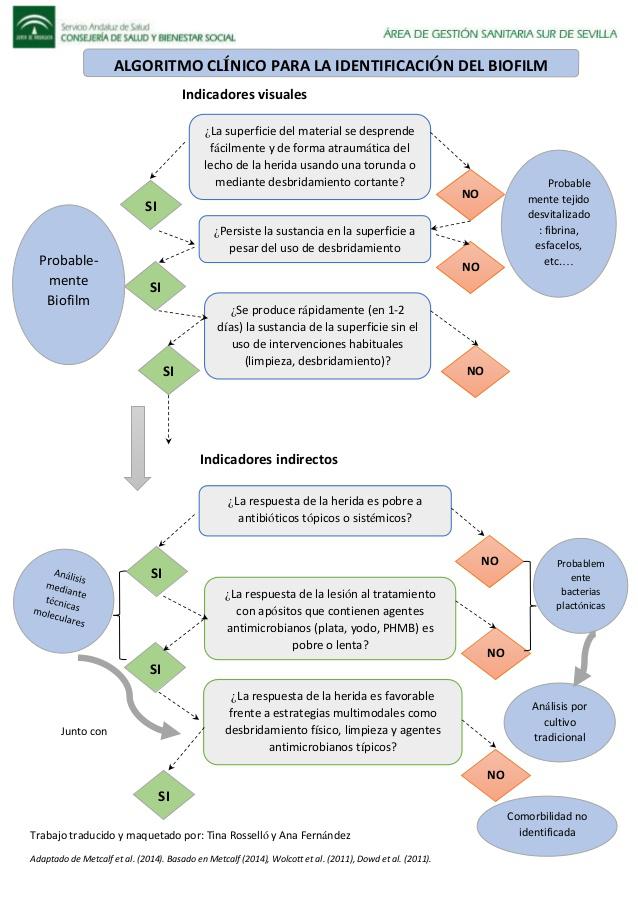
A pesar de que no es del todo fiable detectar el biofilm sin el uso de un microscopio, varios autores recomiendan el uso de algoritmos, como por ejemplo podría ser el Algoritmo de Metcalf.
Biofilm en las heridas crónicas
El tiempo que tardan las colonias de los microorganismos en desarrollar la película protectora, dependiendo del tipo de bacteria/hongo, suele variar entre unos 5-7 días, por lo tanto, es muy importante ser rápidos y precisos a la hora de detectar una infección y tratarla; sobre todo en caso de estas heridas que son las más vulnerables ante las comunidades microbianas. La fragilidad de las heridas crónicas viene dada a que, normalmente, se presentan en pacientes con problemas circulatorios e inmunitarios, que aumentan el riesgo de infección y, al mismo tiempo, reducen la respuesta del organismo ante un patógeno o al tratamiento antibiótico. Tal y como se ha mencionado antes, el biofilm potencia y prolonga la respuesta inflamatoria de una herida, retrasando su cicatrización y la película protectora que constituyen para los microorganismos reduce la eficacia de los tratamientos aplicados para la cura de las heridas.
- ¿Qué medidas hay que tomar ante la presencia del Biofilm en una herida crónica?
Los dos objetivos principales para erradicar el Biofilm de la superficie de una herida serían:- Reducir la carga del Biofilm: esto se conseguirá mediante el desbridamiento mecánico de la herida, eliminando el tejido necrosado y contaminado.
- Evitar que se reconstruya: utilizando apósitos para tapar la herida y protegerla de una sobreinfección; emplear productos antibacterianos en las curas, como podrían ser la plata, pomadas antibióticas y soluciones antimicrobianas de amplio espectro (PHMB, ácido hipocloroso, ozonoterapia, etc.). Este paso también sirve para la prevención de la formación de Biofilm en una herida que se encuentra en fase de riesgo.
Conviene recurrir a un tratamiento antibiótico para combatir la infección y terapia compresiva en caso de las heridas de origen vascular en MMII. El mayor problema que presenta el Biofilm, de vista al futuro, es el aumento de las resistencias que van desarrollando los microorganismos frente a los antimicrobianos y los antibióticos. Durante este proceso, una intervención multidisciplinar será fundamental, dado que las curas del equipo de enfermería tendrán que ser apoyadas por el equipo médico que será el responsable de las pautas de la antibioterapia y participará en la valoración y eliminación del Biofilm.
¿Sigue presente el Biofilm sobre el lecho de la herida?
La respuesta más fiable a esta pregunta nos la aportará la repetición de la prueba de cultivo del tejido/ exudado de la herida.
Los signos que podrían sugerir su desaparición podrían ser la disminución del exudado y esfacelo/ fibrina, buena respuesta al tratamiento y curas. Esta forma de valoración no se considerará como definitiva sin una confirmación por parte del laboratorio.
En conclusión, es de gran importancia saber distinguir bien el lecho de una herida limpia del de una infectada o una con biofilm. El personal de enfermería, encargado de las curas, debería saber detectar la aparición de la biopelícula y tomar las medidas correspondientes para su erradicación y evitar la diseminación de este. Recordar, que el uso de los agentes antimicrobianos de amplio espectro ayudará a evitar la creación de las comunidades de los microorganismos y que puedan llegar a formar el biofilm. Así mismo, la colaboración entre un equipo multidisciplinar nos proporcionará mejores resultados en la resolución de una herida que presenta biofilm y mejorará la fase de prevención de este.
Bibliografia
- Phillips PL, Wolcott RD, Fletcher J, Schultz GS. Biofilms Made Easy. Wounds International 2010; 1(3): Available from http://www.woundsinternational.com
- Unión Mundial de Sociedades de Cicatrización de Heridas (World Union of Wound Healing Societies, WUWHS), Congreso de Florencia, Documento de Posición. Tratamiento del biofilm. Wounds International 2016